北京时间1月29日
清华大学集成电路学院任天令教授团队
提出世界首个柔性存算芯片——FLEXI
实现边缘计算场景高性能算力突破
相关研究成果以《一种用于边缘智能的柔性数字存内计算芯片》为题
在线发表于《自然》(Nature)
2026年以来
清华大学作为第一署名作者的第一单位
共有8项科研成果
在Nature,Science,Cell
三大国际高影响期刊发表
位居全国高校首位
除上述成果外
另外7项成果分别为
药学院刘翔宇副教授课题组
发现通用别构剂
为药物耐受难题提供全新解法
生命科学学院齐天从副教授课题组
与合作者首次发现全新植物快速免疫系统
生命科学学院米达副教授团队与基础医学院郭增才副教授团队
合作实现哺乳动物发育大脑中神经元与
免疫细胞动态的活体观察
生物医学工程学院张明君教授团队
联合攻关突破血脑屏障
让药物直达大脑病灶
生命科学学院米达副教授团队
合作揭示人类大脑抑制性神经元扩增及
多样性产生的关键机制
电子工程系徐丰力助理教授、李勇教授
与合作团队共同揭示AI赋能科研的“内卷悖论”
智能产业研究院(AIR)兰艳艳教授团队联合生命学院张伟副教授、闫创业副教授
化学系刘磊教授
创新研发AI驱动的
超高通量药物虚拟筛选平台DrugCLIP
研发世界首个
柔性存算芯片——FLEXI
北京时间1月29日,集成电路学院任天令教授团队与合作者提出了世界首个柔性存算芯片——FLEXI。相关研究成果以《一种用于边缘智能的柔性数字存内计算芯片》(A flexible digital compute-in-memory chip for edge intelligence)为题在线发表于《自然》(Nature)。

当前,人工智能与物联网、具身智能深度融合,轻量、高效、柔性的智能计算硬件需求迫切。传统硅基刚性芯片无法贴合人体或复杂曲面设备,现有柔性处理器则存在工作频率低、能耗高、缺乏并行计算能力等短板,难以胜任神经网络推理等密集型任务。
FLEXI采用低温多晶硅薄膜晶体管,薄如蝉翼、可随意弯折,且具备超低功耗、高能效、高稳定性和低成本优势。

柔性芯片实物图与三维结构示意图
其“存内计算”架构将“计算单元”嵌入在“存储器”内,大幅提升效率。最小版本FLEXI-1芯片仅31.12平方毫米,可在55.94微瓦超低功耗下运行,能承受4万次以上180度弯曲且性能稳定,单个千比特容量芯片即可实现99.2%准确率的心律失常检测,为下一代可穿戴医疗设备、柔性脑机接口以及智能机器人等提供坚实的硬件基础。
论文链接:
https://www.nature.com/articles/s41586-025-09931-x
为药物耐受难题提供全新解法
北京时间1月27日,药学院刘翔宇课题组在《细胞》(Cell)在线发表题为《通用型别构激动剂稳定的 GPCR-G 蛋白-β-arrestin 超级复合物》(A GPCR-G protein-β-arrestin megacomplex enabled by a versatile allosteric modulator)的研究论文。

G 蛋白偶联受体(GPCRs)是人体基因组中成员最多的膜蛋白受体超家族,也是药物研发中最关键的靶点之一。
本研究通过自主建立的新型 GPCR 药物筛选平台(SPS 方法),首次发现艾滋病临床药物阿扎那韦是一种可作用于多种GPCR的通用型正向别构调节剂(pan-positive allosteric modulator,pan-PAM),并能介导 G 蛋白信号的持续激活。冷冻电镜结构进一步表明,阿扎那韦如同“分子胶水”,促成 GPCR、G 蛋白与 β-arrestin 三者形成超级复合物,使原本对立的 G 蛋白与 β-arrestin 信号通路实现“化敌为友”的共存。这项工作拓展了对 GPCR 信号调控的理解,为创新药物开发提供了全新视角。
论文链接:
https://www.cell.com/cell/abstract/S0092-8674(25)01436-9
首次发现
全新植物快速免疫系统
北京时间1月27日,生命科学学院齐天从副教授课题组与合作者在《细胞》(Cell)发表题为《一个由上游阅读框编码的移动性小肽激活系统性气孔免疫》(An uORF-encoded mobile peptide sparks systemic stomatal immunity)的研究论文。

作为多器官生物,植物在时空上协调全局防御。科学界已知,在病原菌侵染本地叶片后,植物远端未被侵染的叶片经过数天时间可以获得一种依赖于水杨酸途径而持续数天甚至数周的免疫抗性,称为“系统获得性抗性(SAR)”。然而,适宜病原菌侵害的环境往往使植株器官在短期时间(数小时)内先后遭受病原菌威胁。植物是否存在一种快速预警系统,在病原菌侵染本地叶片后,迅速将免疫信息传递至远端未被侵染的叶片,提前统筹防御,赋予植物全局性免疫能力。这是一个亟待解决的关键科学问题。

“系统性气孔免疫”通路模式图
本研究首次发现了一种侵染早期快速启动的全新全局性免疫系统“系统性气孔免疫”,鉴定了介导该系统的移动性信号分子及其受体复合体,揭示了新型的细胞内信号转导机制,阐明了病原菌侵染早期快速启动全局防御的分子通路。
“系统性气孔免疫”这一全新防御系统,区别于建立缓慢的“系统获得性抗性”,也不依赖于水杨酸通路,而是以一种更精简、更迅速的信号转导特性,实现植物全身的整体性防御。这一发现不仅开拓了植物免疫学理论,也为开发广谱、快速抗病特性的作物提供了重要理论基础。
论文链接:
https://www.cell.com/cell/fulltext/S0092-8674(25)01437-0
实现哺乳动物发育大脑中神经元与
免疫细胞动态的活体观察
北京时间1月22日,生命科学学院米达副教授团队与基础医学院郭增才副教授团队合作,在《细胞》(Cell)发表了题为《哺乳动物发育大脑中神经元与免疫细胞动态的活体观察》(Intravital observation of neuronal and immune cell dynamics in the developing mammalian brain)的研究论文。

传统基于急性脑切片成像的研究会破坏大脑完整性、脑内血管网络以及免疫细胞的生理静息状态,加之现有胚胎活体成像技术在观测稳定性、视角多样性和操作便捷性等方面的局限,使得在体观测胚胎小鼠大脑中神经细胞动态行为面临重大挑战。

研究总结图
本研究综合应用新型胚胎小鼠活体成像技术IMEE、活体血管标记与向量场拓扑分析等方法,系统阐明了哺乳动物胚胎大脑内不同类型神经元与免疫细胞的动态行为,首次揭示了迁移神经元与血管网络、小胶质细胞之间的动态互作模式,并展示了病理条件下细胞行为的异常与响应。该工作为深入理解大脑发育过程中细胞对周围环境的适应机制提供了重要实验证据和理论依据,也为研究发育性脑疾病的致病机制提供了全新方法。
论文链接:
https://www.cell.com/cell/fulltext/S0092-8674(25)01313-3
突破血脑屏障
让药物直达大脑病灶
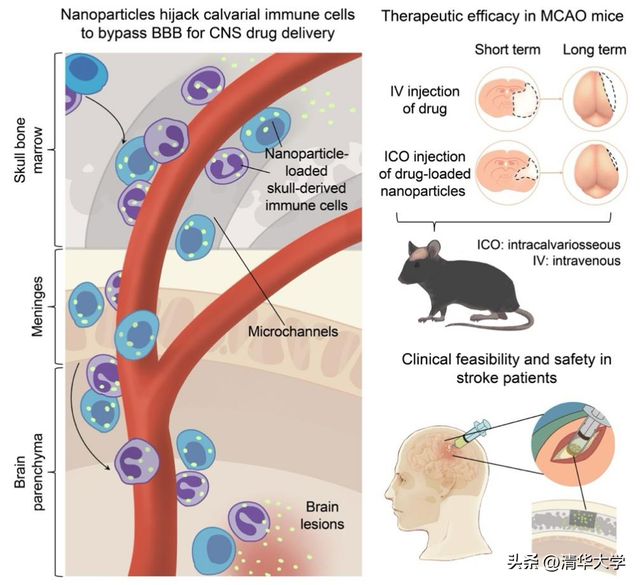
北京时间1月16日,生物医学工程学院张明君教授团队与合作者联合攻关,绕过血脑屏障,利用载药纳米颗粒“劫持”颅骨骨髓免疫细胞,借助其在颅骨-大脑之间的天然迁移通路,将药物精准递送至脑卒中病灶。相关研究成果以《纳米颗粒劫持颅骨骨髓免疫细胞用于CNS药物递送和卒中治疗》(Nanoparticles hijack calvarial immune cells for CNS drug delivery and stroke therapy)为题,在线发表于《细胞》(Cell)。
血脑屏障严格调控血液与大脑间物质通行,将绝大多数药物阻隔,是脑神经疾病新药研发的主要瓶颈之一。研究团队通过颅骨骨髓微创注射,将载药白蛋白纳米颗粒送入颅骨骨髓腔,其可被免疫细胞高效摄取,且该系统在体内暴露极低,几乎进入不了外周血液和主要脏器,更不会影响免疫细胞活力,生物安全性良好。
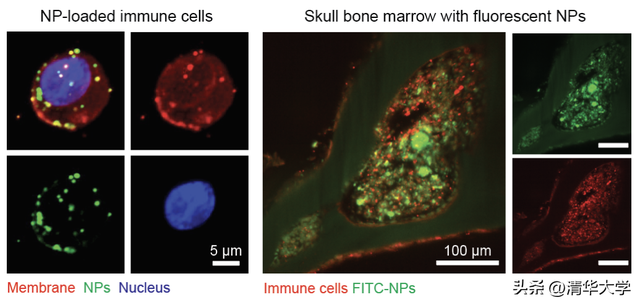
经颅注射纳米颗粒被免疫细胞高效摄取
未来该通路不止于药物递送,作为微创高效的脑部生物物料传输通道,有望与脑机接口深度融合,成为承载“物料流、能量流、信息流”的多方位交互接口,打破大脑与人工系统的交互屏障,借助微纳机器人实现药物闭环递送,为脑机智能融合研究提供新思路。
论文链接:
https://www.cell.com/cell/fulltext/S0092-8674(25)01421-7?sessionid=252235806
揭示人类大脑抑制性
神经元扩增及多样性
产生的关键机制
北京时间1月15日,生命科学学院米达副教授团队合作在《科学》(Science)发表了题为《脑室下区放射状胶质细胞维持人脑抑制性神经元的持续产生》(Subventricular zone radial glial cells maintain inhibitory neuron production in the human brain)的研究论文。

该研究聚焦人脑动态发育过程,基于珍贵样本系统绘制了人类大脑内侧神经节隆起(MGE)脑区的细胞发育图谱,首次在人类胎儿大脑中发现了一类独特的神经干细胞类型——SVZ RGC(脑室下区放射状胶质细胞),并揭示SVZ RGC在人类妊娠期中持续产生抑制性神经元和神经胶质细胞,从而增加了人类大脑皮层抑制性神经元的数量及比例。
该研究为深入理解人类特有的大脑抑制性神经元发育机制和在进化上大脑皮层扩张机制提供了重要理论基础。鉴于抑制性神经元的功能缺陷与癫痫、自闭症等多种神经系统疾病密切相关,这类新型神经干细胞的发现将为制定未来相关疾病的潜在干预策略开辟新的方向。
论文链接:
https://doi.org/10.1126/science.adw1803
揭示AI赋能科研的“内卷悖论”
北京时间1月14日,电子工程系徐丰力助理教授、李勇教授与合作团队,首次揭示了AI在助力科学家加速自身研究进展的同时,却导致科学界的集体注意力窄化和趋同探索的矛盾效应。相关研究成果以《人工智能促进科学家影响力增长却制约科学认知边界扩张》(Artificial intelligence tools expand scientists’ impact but contract science’s focus)为题,在线发表于《自然》(Nature)。

这一矛盾机制的发现,是对AI赋能科研模式的深度反思。现有的AI for Science,虽然极大地促进了局部的效率提升,却难以驱动全链条、多领域的科研创新。正是这种局限性,导致AI倾向于在既有数据上深入挖掘,而非在未知领域开辟探索全新问题。

科学探索的 “群体登山” 效应
为突破这一局限,团队提出“全流程科研智能体系统”(OmniScientist.ai),推动AI从 “辅助工具” 进化为具备 “主动提出假说、自主设计实验、分析结果并形成理论” 的 “AI科学家”。通过人机深度融合和协同,形成超级智能体,拓展认知边界、催生颠覆性科学理论。
论文链接:
https://www.nature.com/articles/s41586-025-09922-y
AI助力药物虚拟筛选
提速百万倍
北京时间1月9日,智能产业研究院(AIR)兰艳艳教授团队联合生命学院张伟副教授、闫创业副教授,化学系刘磊教授创新研发AI驱动的超高通量药物虚拟筛选平台DrugCLIP,比传统方法实现了百万倍提升,在预测准确率上也取得显著突破。相关研究成果以《深度对比学习实现基因组级别药物虚拟筛选》(Deep contrastive learning enables genome-wide virtual screening)为题,在线发表于《科学》(Science)。

目前,受限于高通量实体筛选技术与传统分子对接技术的高昂成本,绝大多数潜在靶点和化合物仍未被充分探索。DrugCLIP将原本需要数百年才可完成的计算量,缩短为一台计算节点一天的机时,并首次打通了从蛋白结构预测到药物发现的关键通道,实现覆盖人类基因组规模的虚拟筛选。

DrugCLIP主页
依托DrugCLIP,联合团队首次完成了人类基因组规模的虚拟筛选项目,可覆盖约1万个蛋白靶点、2万个蛋白口袋,分析筛选超过5亿个类药小分子,总共富集出超过200万个潜在活性分子,构建了目前已知最大规模的蛋白-配体筛选数据库,该数据库已免费面向全球科研社区开放,为基础研究与早期药物发现提供了强大数据支持。
论文链接:
https://www.science.org/doi/10.1126/science.ads9530





